鉴定出可阻断有毒形式的帕金森氏症相关蛋白的天然人类分子
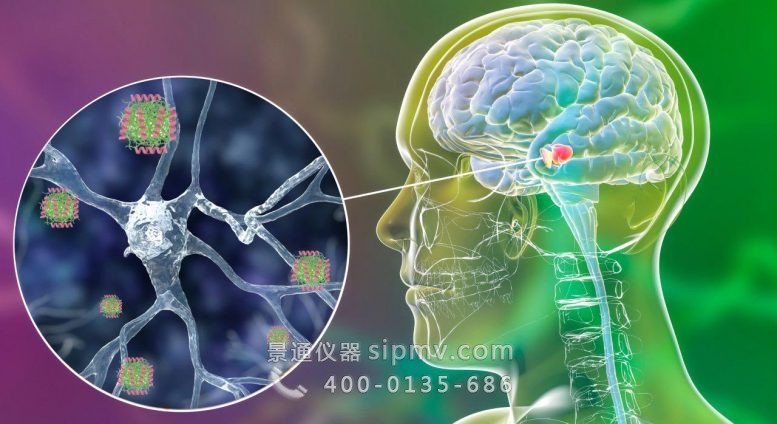
人肽 LL37 与 α-突触核蛋白的毒性低聚物结合、阻断其传播并防止其神经毒性的示意图。图片来源:Irantzu Pallarès,IBB-UAB
UAB 和 UniZar 的研究人员已经确定了一种在大脑中发现的人类肽,它可以阻断与帕金森病相关的 α-突触核蛋白聚集体并防止其神经毒性。这项发表在《自然通讯》上的研究表明,这可能是生物体对抗聚集的自然机制之一。这一发现可能有助于为帕金森病和其他突触核蛋白病理开发新的治疗和诊断策略。
专门合成多巴胺(大脑的主要神经递质之一)的神经元的死亡会降低帕金森病患者的运动和认知能力。这些神经元的损失与α-突触核蛋白聚集有关。最近的研究表明,寡聚体是这种蛋白质的初始聚集体,是 α-突触核蛋白最具致病性的形式,是导致疾病在大脑中传播的原因。
因此,对抗这种疾病的更有希望的方法之一在于中和这些寡聚体,从而减缓病理进展。然而,这些聚集体不呈现明确的结构并且它们本质上是暂时的,这一事实使得识别具有足够强度结合以探索任何临床应用的分子变得极其困难。
相关仪器推荐: 摄像头/相机接口
巴塞罗那自治大学 (UAB) 的生物技术和生物医学研究所 (IBB) 和萨拉戈萨大学 (UniZar) 的生物计算与系统综合研究所 (BIFI) 的研究人员之间的科学合作现在已经能够鉴定一种与 α-突触核蛋白寡聚体强烈且特异性结合的人类内源性肽,从而避免它们的聚集并阻断它们的神经毒性,这两个过程与帕金森病的神经退行性衰退密切相关。该肽的鉴定和研究称为 LL-37,最近发表在Nature Communications上。
“LL-37以选择性方式与有毒的α-突触核蛋白寡聚体相互作用,其强度优于先前描述的任何肽,相当于抗体表现出的强度。研究人员指出,它在非常低的浓度下抑制聚集并保护神经元细胞免受损害。
他们补充说,“LL-37 天然存在于人类有机体中,包括大脑和肠道,在帕金森病中发生 α-突触核蛋白聚集的器官。这表明 LL-37 的活性可能对身体自身开发的一种机制做出反应,作为自然对抗这种疾病的一种手段。”
受到这一想法的鼓舞,研究人员现在想要研究如何调节其表达,以及这种策略是否可以成为一种有可能影响疾病进程的安全疗法。IBB 研究员兼该研究协调员 Salvador Ventura 表示:“帕金森病的治疗方法可能已经存在于我们的内部,并且只需要正确激活即可。”
LL-37 的鉴定是在分析致病性寡聚体的结构和特征的研究框架下进行的,目的是以特定方式中和它们。进行的分析表明,具有疏水侧和另一个带正电侧的螺旋肽非常适合这种类型的活性。这些试验使研究人员能够鉴定出三种具有抗聚集活性的分子:除了人类分子之外,还鉴定了细菌中存在的第二种肽和第三种人工制造的分子。
除了代表帕金森病和其他突触核蛋白病理的可能治疗途径外,研究中鉴定的分子是其诊断的有希望的工具,因为它们可以区分功能性和毒性 α-突触核蛋白种类。
“到目前为止,还没有分子能够选择性和有效地识别有毒的 α-突触核蛋白聚集体;我们在这些问题上提出的肽是独一无二的,因此具有作为诊断和预后工具的巨大潜力,”BIFI-UniZar 研究员、研究协调员 Nunilo Cremades 说。
在这项研究中,计算分析了超过 25,000 种人类肽,并应用了单分子光谱学方法以及蛋白质工程,以及使用有毒低聚物的体外细胞培养。
类似内容推荐
- 研究发现一些导致疾病的真菌会通过微小的间隙生长
- 红细胞中的抗衰老蛋白有助于预防精神衰退、记忆力差和听力缺陷
- 科学家尝试使用核磁共振波谱 (NMR)构建SARS-CoV-2分子的三维结构
- 研究人员开发了一种深度学习模型可使用单个3D MRI扫描将脑肿瘤分类
- 研究发现抗生素可以治疗癌症等人类疾病
- 新诊断策略可用来作为帕金森病和其他突触核蛋白病理治疗
- 科学家们发现了变异的冠状病毒蛋白复合物
- 生命起源的新认识:研究人员首次创造出可复制的RNA分子
- 研究人员发现数百种可能影响囊性纤维化的新蛋白质
- 能够感应和改变细胞生物电场的纳米级分子装置首次问世
- 普利兹克分子工程学院研究的药物有望对抗变异新冠病毒
- 分子影像展示了氯离子进入细胞的过程
- 蛋白质控制在帕金森病中出错的线粒体裂变过程
- 独特的电子显微镜可拍摄运动中的分子
- 荧光显微镜串色了,紫外通道(DAPI)能看到CFP(青色荧光蛋白),怎么办?
- 共焦显微镜或推动青光眼医疗进展
- 日本研发彩色医疗电子显微镜 有助癌症早期诊断
版权属于:景通仪器 - 国内领先的显微镜与显微数字成像解决方案供应商
转载时必须以链接形式注明作者和原始出处及本声明。
本文地址:http://www.sipmv.com/blog/3393/